Forse è la volta buona. Il meccanismo biologico che sta alla base della schizofrenia, il più enigmatico dei disturbi psichici, sembra essere stato individuato, almeno a grandi linee. Uno studio pubblicato online su Nature il 27 gennaio! a cura di Steven McCarroll, associate professor of genetics at Harvard e Beth Stevens, assistant professor of neurology at Boston Children’s Hospital and Harvard, è riuscito a dimostrare quale gene e quale processo neurobiologico sarebbero responsabili per l’insorgenza di questa malattia che colpisce circa l’1% della popolazione e di cui hanno sofferto personaggi illustri quali, tra gli altri, Hölderlin, Strindberg, John Nash (mirabilmente ritratto in Beautiful Mind) e meno, All The Madmen cui Bowie dedicava il suo brano. Anche se la scoperta non porta al momento con sé una nuova cura o un nuovo test diagnostico, segna, a detta di molti esperti, una (prima) pietra miliare nella comprensione di un disturbo psichico, caratterizzato tra l’altro da deliri e allucinazioni, per il quale le cure sono spesso ancora non risolutive.
Impressionante il lavoro che sta alle spalle di questo brillante risultato: l’analisi, durata cinque anni, del genoma di quasi 65.000 persone e una paziente e geniale opera di costruzione di un mosaico scientifico con tasselli che provengono dai campi della genetica, della psichiatria e della neurologia.
I ricercatori sono riusciti a dimostrare che il rischio di schizofrenia è strettamente legato al processo di “potatura sinaptica” (synaptic pruning) al taglio cioè delle connessioni superflue tra cellule nervose. Tale processo di “potatura” avviene normalmente fintanto che il cervello sta ancora maturando, nella fase cioè del l’adolescenza e della prima giovinezza, che è anche l’età di più comune insorgenza della schizofrenia. In questa fase il processo di potatura riguarda principalmente le aree cerebrali preposte al pensiero, alla progettazione delle azioni e all’elaborazione critica, la cosiddetta corteccia pre-frontale. Nei pazienti affetti da schizofrenia queste aree cerebrali presentano molte meno connessioni tra cellule nervose che nei soggetti normali. Lo studio ha dimostrato che ciò avviene a causa di un eccesso di “potatura”. Più precisamente, soggetti con un difetto genetico andrebbero incontro ad una potatura sinaptica troppo forte con conseguente impoverimento delle connessioni (sinapsi) tra cellule nervose (nella corteccia prefrontale) e relativi sintomi a carico del pensiero (deliri), delle capacità critiche (alterazione del senso di realtà e della capacità di giudizio) del comportamento etc.
Ma come sono arrivati i ricercatori a queste conclusioni?
Un passo alla volta.
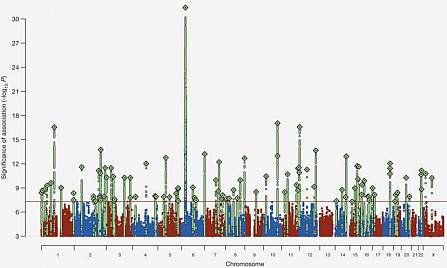
Quando ormai sedici anni fa è stato identificato il genoma umano si era sperato di identificare, tra gli altri, anche i geni della schizofrenia. Speranza andata allora però delusa. Con il successivo avvento tuttavia di studi di associazione genomica su vasta scala (GWAS) è stato possibile individuare (nel 2014) ben 108 regioni genetiche (loci) associate con un rischio di schizofrenia. Ma quali quelle davvero decisive? La più forte associazione per la schizofrenia è stata trovata su una regione del cromosoma 6 che contiene geni coinvolti nel processo di risposta immunitaria, il cosiddetto complesso maggiore di istocompatibilità MHC. (Nella grafica riportata sopra – detta Manhattan plot per la somiglianza con i grattacieli della zona – il MHC è la statua della libertà, la guglia più alta). Ma qui le malattie auto-immuni non c’entrano. Si è visto invece che all’interno del MHC i rischi maggiori erano associati con il gene C4, un fattore di complemento, che può esistere in quattro forme diverse e produce due proteine diverse C4-A e C4-B.
A questo punto i ricercatori hanno analizzato il genoma di quasi 65.000 persone! e hanno constatato che i soggetti affetti da schizofrenia avevano più frequentemente la variante C4A, e ciò in misura statisticamente assai significativa.
“C4-A seemed to be the gene driving risk for schizophrenia”
Ma perché? si sono chiesti.
E qui sono stati utili studi neurologici già noti, ma mai finora collegati al tema della schizofrenia. Già nel 2007 Beth Stevens aveva dimostrato che le proteine prodotte da geni situati sul MHC erano coinvolte nel processo di potatura sinaptica nel normale sviluppo del cervello. Topi allevati senza geni C4 presentavano alterazioni molto gravi dei processi di potatura sinaptica. D’altro canto un eccesso di proteina C4-A determina tagli troppo severi e dannosi delle connessioni sinaptiche proprio nella fase più delicata dello sviluppo cerebrale. La Dr. Steven conclude dunque:
“the evidence strongly suggested that too much C4-A leads to inappropriate pruning during this critical phase of development.”
Riassumendo, i soggetti con la variante genetica C4A producono un eccesso di proteina C4-A che a sua volta determina un’eccessiva e dannosa potatura sinaptica, il che si traduce in un assottigliamento delle connessioni neuronali a livello della corteccia frontale con relativi disturbi psichici. Ciò spiega al tempo stesso il perché dell’insorgenza della malattia nella fase di maturazione cerebrale, adolescenza e prima giovinezza.
Gli autori concludono dunque
“The finding connects all these dots, all these disconnected observations about schizophrenia, and makes them make sense,”
Ma il Dr. Lander averte anche
“I’m not ready to call it a victory until we have something that can help patients”
Infine qualche considerazione personale:
Dopo tanti annunci vani e speranze deluse, questa appare, per rigore scientifico e capacità di unificare con elegante semplicità, aspetti clinici e risultati biologici diversi, una tappa fondamentale per comprendere la schizofrenia e in un futuro speriamo non troppo lontano diagnosticarla precocemente e curarla efficacemente.
Lo studio in questione è anche la migliore dimostrazione che convergence science e il conseguente effetto Medici sono la strategia più efficace, soprattutto in ambito di neuroscienze, per affrontare e risolvere problemi e disturbi complessi. Superare le (antiche e stupide) rivalità e incomprensioni tra discipline diverse (psichiatria, psicoanalisi, psicologia cognitiva, neurologia, neuro diagnostica, genetica,…), nel rispetto delle specifiche competenze, non può che giovare ai pazienti, ai quali servono tanto le analisi neurobiologiche quanto il dialogo. Per sconfiggere un orrore che Zelda Fitzgerald, ricoverata per schizofrenia, nel suo epistolario con il marito Scott così descrive:
“Un distacco come se fossi stata dall’altra parte di un velo nero… Ma perfino questo era meglio del guscio vuoto, infantile vacillante che sono adesso. Ho tanta paura che quando vieni e trovi che non rimane altro che vuoto e disordine ti farà orrore” (da Caro Scott, Carissima Zelda, a cura di Jackson R. Bryer e Cathy W. Barks, La Tartaruga)
Suggerimento sonoro: Opening schizophrenia’s black box
Immagine tratta da:Schizophrenia’s strongest known genetic risk deconstructed | National Institutes of Health (NIH)